meckpomm-abi2014-chemie-lehrerhinweise.pdf
Dieses Dokument ist Teil der Anfrage „Abitur-Aufgaben im Fach Chemie im Jahr 2014 in Mecklenburg-Vorpommern“
Diese Anfrage wurde als Teil der Kampagne „Frag sie Abi!“ gestellt.
Mecklenburg-Vorpommern Zentralabitur 2014 Chemie Hinweise für den Lehrer (nicht für die Hand des Prüflings)

Seite 2 Abitur 2014 Chemie (Lehrer) Hinweise für den Lehrer Hinweise zur Prüfung: Aufgabenauswahl: Von den 2 Aufgabenblöcken I und II ist nur einer zu bearbeiten. TeilAdes gewählten Aufgabenblockes bearbeiten alle Schüler. Teil B wird nur von den Prüflingen bearbeitet, die auf erhöh- tem Anforderungsniveau geprüft werden. Bearbeitungszeit: Die Arbeitszeit für den Teil A beträgt 240 Minuten. Die Ar- beitszeit für die Teile A und B beträgt 300 Minuten. Zusätz- lich stehen allen Schülerinnen und Schülern 30 Minuten für die Wahl des Aufgabenblockes zur Verfügung. Hilfsmittel: - an der Schule zugelassener Taschenrechner - an der Schule verwendetes Tafelwerk - Duden zur deutschen Rechtschreibung Schülerinnen und Schüler, deren Muttersprache nicht die deutsche Sprache ist, können als zusätzliches Hilfsmittel ein zweisprachiges Wörterbuch in gedruckter Form verwenden. Näheres regelt die Schule. Für die Berechnungen wurden die Werte aus dem Duden-Paetec-Tafelwerk zugrun- de gelegt. Die chemische Zeichensprache und die chemischen Gesetzmäßigkeiten sind in angemessener Form anzuwenden, auch wenn es die Aufgabenstellung nicht unmittelbar fordert. Die Lösungen sind in sprachlich einwandfreier Form darzustellen und die Ergebnisse der Berechnungen sind in einem sinnvollen Antwortsatz zu formulieren. Alle Prüfungsunterlagen sind geschlossen nach Ablauf der schriftlichen Prüfung einzusammeln. Hinweise zur Korrektur und Bewertung: Die Bewertung der Leistungen orientiert sich an der Beschreibung der erwarteten Prüfungsleistung in Verbindung mit den vorgesehenen Bewertungseinheiten (Erwartungshorizont) und geht von den Anforderungen der Aufgabenstellung sowie den unterrichtlichen Voraussetzungen aus. Damit unterliegt die Bewertung der besonderen Verantwortung der Beurteilenden. Die Leistung des Prüflings ist grundsätzlich als Ganzes zu würdigen. Löst der Prüf- ling eine Aufgabe in besonderer Qualität und über das im Erwartungshorizont skiz- zierte Maß hinaus, kann eine zusätzliche Bewertungseinheit erteilt werden. Insgesamt sind pro Arbeit maximal 2 zusätzliche Bewertungseinheiten möglich, wobei die Erteilung in der Korrektur begründet werden muss und die Summe von 40 bzw. 60 Bewertungseinheiten nicht überschritten werden darf.

Abitur 2014 Chemie (Lehrer) Seite 3 Nicht im Erwartungshorizont aufgeführte Lösungswege sind bei der Bewertung an- gemessen zu berücksichtigen, sofern sie im Rahmen der Aufgabenstellung liegen. Wiederholungsfehler werden in der Regel nur einmal gewertet, wenn die Lösung chemisch sinnvoll bleibt. ln Grenzfällen muss das Nichterteilen von Bewertungseinheiten ebenso begründet werden wie das Erteilen. Bei der Korrektur werden in sachlich wertenden Randvermerken Vorzüge und Mängel der Arbeit im inhaltlichen, sprachlichen und methodischen Bereich gekenn- zeichnet und kommentiert. Dazu gehören: das Vermögen, die Aufgabenstellung zu erfassen die angemessene Verwendung der chemischen Zeichensprache und chemi- scher Gesetzmäßigkeiten die Genauigkeit und Umfang der Kenntnisse und die Klarheit der Einsichten die Sicherheit in der Anwendung der Arbeitstechniken, der Verfahren und der Fachsprache die Folgerichtigkeit und Differenziertheit der Aussagen die Herausarbeitung des Wesentlichen das Anspruchsniveau der Problemerfassung die Fähigkeit des Prüflings, die Bedingtheit und Tragwe ite eigener und fremder Aussagen kritisch zu würdigen die Breite der Argumentationsbasis die zusammenhängende und sprachlich korrekte Darstellung die sinnvolle Formulierung von Antwortsätzen bei Berechnungen die Klarheit und Eindeutigkeit der Aussagen die Angemessenheit der Darstellung die Klarheit der Gliederung und der inhaltlichen Ordnung. Entwürfe können ergänzend zur Bewertung nur herangezogen werden, wenn sie zusammenhängend konzipiert sind und die Reinschrift etwa Dreiviertel des erkenn- bar angestrebten Gesamtumfanges entspricht. BE grundlegendes Anforderungsniveau 38-40 36-37 34-35 32-33 30-31 28-29 26-27 24-25 22-23 20-21 18-19 14-17 11-13 07-10 04-06 Zensuren- punkte 15 14 13 12 11 10 09 08 07 06 05 04 03 02 01 BE erhöhtes Anfor- derunsniveau 57-60 54-56 51-53 48-50 45-47 42-44 39-41 36-38 33-35 30-32 27-29 22-26 16-21 11-15 05-10 Zensuren- punkte 15 14 13 12 11 10 09 08 07 06 05 04 03 02 01
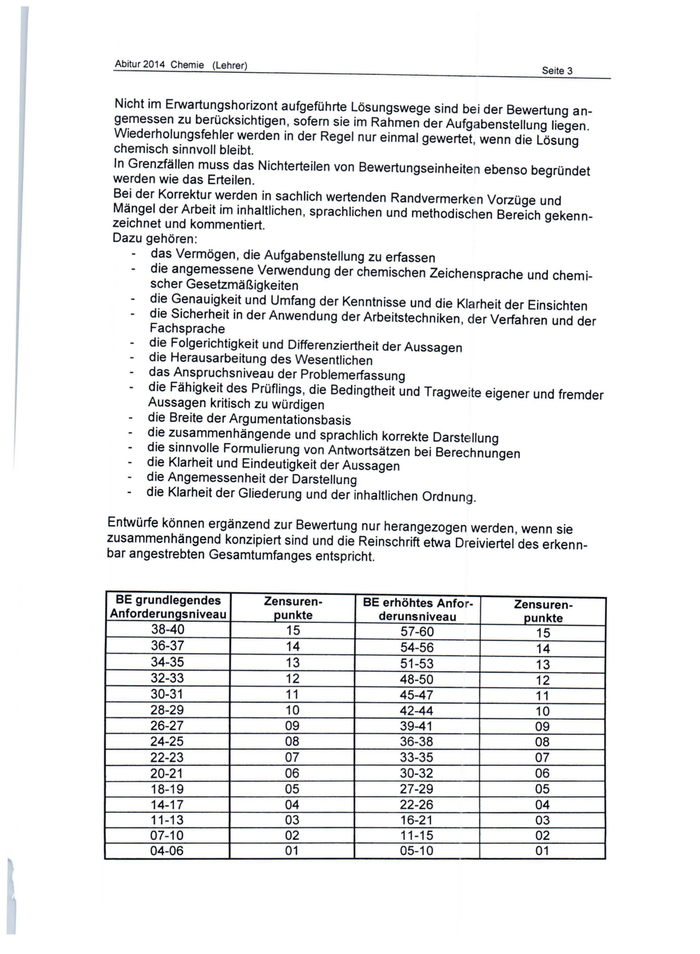
Abitur 2014 Chemie (Lehrer) Seite 4 Block I Höhlenchemie BE Aufgabenblock I Teil A 1.1 1.2 1.3 1.4 1.5 Erläuterung, Ableitung der Eigenschaften Formulierung des MWG, Nennen und Begründen Berechnung; V(C02) = 6,72 I Reaktionsgleichung, Berechnung : V(H20) 283 I Experiment: Protokoll 6 3 3 3 6 2.1 2.2 Bestimmung, Berechnung m(C2H2) = 100 g 1 1 Berechnung : .0-RHm =- 2508 kJ·mor ; Wm = 2,45 kJ·mor Erläuterung , graphischen Darstellung Diskussion 1 Erläuterung, Berechnung: c(HC0 3-) = 3,03 · 10-4 mol· r 4 7 2.3 2.4 = insgesamt 3.1 3.2 3.3 3.4 3.5 Aufgabenblock I Teil B Elektronenkonfigurationen, Aussage zur Stabilität mit Begründung Erläuterung, Angabe der Vorgänge an den Elektroden, 2 3 Berechnung: E(Ni +/Ni +) = 0,32 V , Wertung Skizze mit Beschriftung Beschreibung und Begründung der Vorgänge Berechnung: t- 10,1 h (= 606 min) Erklärung, Reaktionsgleichungen Anforderungs- bereiche 111 I II 3 3 2 1 3 1 2 4 2 2 2 2 4 1 2 6 3 1 2 1 1 40 11 23 6 2 1 2 2 3 6 2 5 5 2 2 2 2 36 11 4 insgesamt: 60 13
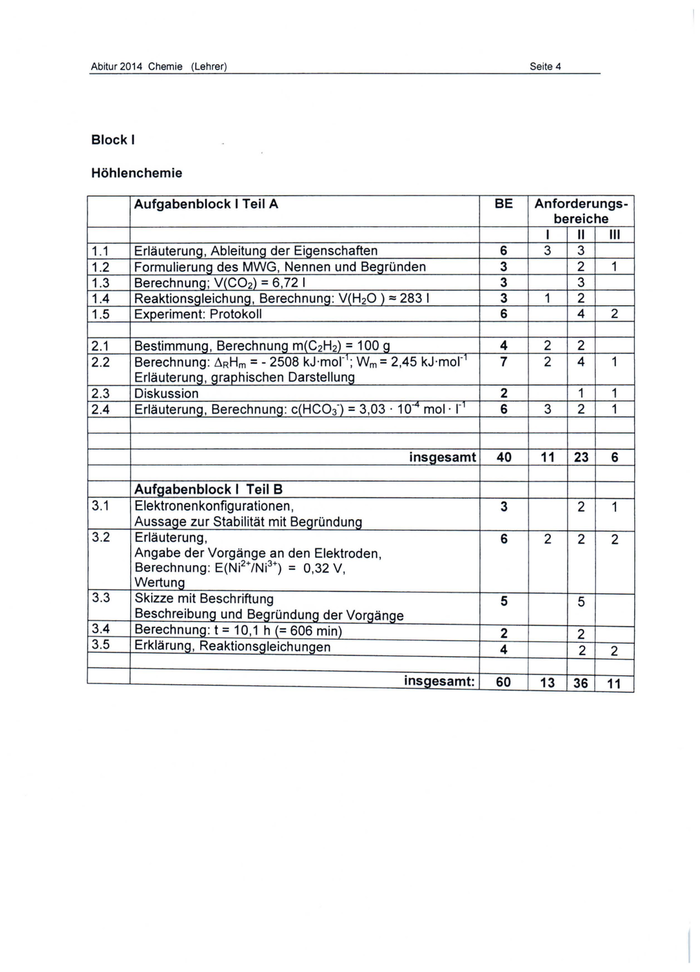
Seite 5 Abitur 2014 Chemie (Lehrer) Block II Heilende Moleküle Aufgabenblock II Teil A 1.1 1.2 1.3 1.4 1.5 2.1 2.2 2.3 Reaktionsgleichungen, Reaktionsart, Begründung Reaktionsgleichung, Berechnung: I= 7·10-o mol · Begründung Grafische Darstellung, Interpretation, Hypothese Berechnung: n(KCI) 8 · 10-;j mol, m(KCI) = 0,6g Planung und Durchführung des Experiments, Protokoll Begründung Erläuterung, Beschreibung, 1 Berechnung: .:1HH -705 kJ· mor ; 1 1 L1GH -710 kJ· mor ; L1LH 5 kJ· mor Entscheidung Begründung 3.1 = 4 3 2 5 4 8 3 9 Anforderungs- bereiche II 111 I 2 2 1 2 2 1 2 2 2 2 2 4 2 1 2 2 4 3 40 12 2 22 6 6 2 4 3 4 4 3 60 1 = Aufgabenblock II Teil B Reaktionsgleichungen, Reaktionsart, Begründung, Berechnung: m(Essigsäure) 13333 t 4 m(Salicylsäure) 3,07· 10 t Reaktionsgleichung, Erklärung Berechnung: pH = 2,6, Erläuterung Erklärung Nennen, Reaktionsgleichung insgesamt: = 3.2 3.3 3.4 3.5 r 1 = = 2.4 BE = 2 1 16 3 3 2 34 2 1 1 10







