CH10_x_G_HT_GG.pdf
Dieses Dokument ist Teil der Anfrage „Abitur-Aufgaben im Fach Chemie im Jahr 2010 in Nordrhein-Westfalen“
CH GK HT 1 Seite 1 von 3 Name: _______________________ Abiturprüfung 2010 Chemie, Grundkurs Aufgabenstellung: Regenwasser vom Kupferdach für den Gartenteich? 1. Erklären Sie die Beobachtungen beim Betrieb der Vorrichtung zum Entkupfern des Regen- wassers. Erklären Sie unter Verwendung entsprechender Fachbegriffe und Reaktions- gleichungen die Funktionsweise dieser Vorrichtung. Prüfen Sie unter Berücksichtigung elektrochemischer und ökologischer Aspekte, ob auch Aluminiumfolie als Füllung für die Vorrichtung zum Entkupfern geeignet ist. (24 Punkte) 2. Geben Sie eine mathematische Beziehung zur Bestimmung der Kupfer-Ionen-Konzen- tration im Wasser an. Berechnen Sie die Spannung der Kupfer-Konzentrationskette für eine Kupfer-Ionen-Konzentration, die empfindliche Fische schädigen kann. Ermitteln Sie, ob das vom Dach ablaufende Regenwasser vor bzw. nach Entkupferung zur Füllung des Gartenteiches geeignet ist. (16 Punkte) 3. Erläutern Sie die Beobachtungen bei Betrieb des elektronischen Gerätes mithilfe von Reaktionsgleichungen. Erläutern Sie, ob die Verwendung von entkupfertem Zisternen- wasser oder der Einsatz eines elektronischen Gerätes hinsichtlich Wirksamkeit und Wartungsaufwand besser zur Algenbekämpfung im Gartenteich geeignet ist. (20 Punkte) Zugelassene Hilfsmittel: Wissenschaftlicher Taschenrechner Periodensystem Wörterbuch zur deutschen Rechtschreibung Nur für den Dienstgebrauch!

CH GK HT 1 Seite 2 von 3 Name: _______________________ Fachspezifische Vorgaben: Kupfer von Kupferdächern wird durch Luft allmählich unter Bildung von braunen, später grünlichen Kupfer-Verbindungen oxidiert. Regenwasser löst einen Teil der so gebildeten Verbindungen, sodass es anschließend Kupfer-Ionen enthält. Der Besitzer eines Hauses mit Kupferdach fängt sein Regenwasser in einer Zisterne (Regen- tonne) auf und möchte mit diesem Wasser regelmäßig seinen Gartenteich füllen. In geringer Konzentration sind Kupfer-Ionen vor allem für Algen giftig – eine willkommene Wirkung, denn so wird der Teich algenfrei und das Wasser klar. Ab einer Massenkonzentration von 2+ β(Cu ) = 0,1 mg/L können empfindliche Fische geschädigt werden. Das Zisternenwasser darf daher keine höhere Kupfer-Ionen-Konzentration aufweisen. Eine grobe Messung mit Kupfer-Teststreifen ergibt, dass die Kupfer-Ionen-Konzentration im Zisternenwasser zwischen 0,5 mg/L und 10 mg/L liegt. Trotz der Messunsicherheit steht fest, dass die Kupfer-Ionen-Konzentration gesenkt werden muss. Dazu wird das Wasser durch die abgebilde- te Vorrichtung geleitet. Durch Kontakt mit der Eisenwolle soll die Kupfer-Ionen-Konzentration im Wasser so abgesenkt werden, dass Fische nicht gefährdet werden. Zulauf von Zisternenwasser Eisenwolle Bei Zulauf von Zisternenwasser bildet sich auf der Eisenwolle rasch ein rötlicher Belag. Nach einiger Zeit zerfällt die Eisenwolle, zurück bleibt nur ein rötlicher Feststoff. Um die Konzentration der Kupfer-Ionen im aus- laufenden Wasser genauer zu messen, wird eine Kupfer-Konzentrationskette verwendet: Auslauf Abbildung 1: Längsschnitt durch die Vor- richtung zur Entkupferung In der Messhalbzelle wird eine Kupfer-Elektrode im Zisternenwasser vor bzw. nach Ent- kupferung eingesetzt; als Referenzhalbzelle dient eine Kupfer-Elektrode in Kupfersulfat- Lösung mit c(CuSO4) = 0,1 mol/L. Die Messung ergibt Spannungen von Uvorher = 0,106 V bzw. Unachher = 0,189 V. Zur Algenbekämpfung in Gartenteichen wird auch ein elektronisches Gerät angeboten, bei dem eine Kupfer-Elektrode als Anode und eine Edelstahl-Elektrode als Kathode geschaltet werden. Zwischen den Elektroden wird eine Spannung so angelegt, dass die Kupfer-Ionen- Konzentration im Teichwasser (pH = 6,8) auf 0,2 bis 0,3 mg/L ansteigt. An der Kathode tritt dabei eine Gasentwicklung auf. Laut Hersteller ist diese Kupfer-Ionen-Konzentration für Menschen, Tiere und Pflanzen absolut unbedenklich, da der für Trinkwasser zulässige Grenzwert von 2 mg/L nicht erreicht wird. Nur für den Dienstgebrauch!

CH GK HT 1 Seite 3 von 3 Name: _______________________ Zusatzinformationen: Wirkung und Grenzwerte für Metall-Ionen in Wasser Al 3+ fischgiftig ab β(Al ) = 0,1 mg/L 3+ giftig für Pflanzen ab β(Al ) = 0,2 mg/L 2+ schädigt Algen ab β(Cu ) = 0,002 mg/L 2+ 2+ -6 schädigt empfindliche Fische ab β(Cu ) = 0,1 mg/L (c(Cu ) = 1,57 ·10 mol/L) 2+ wichtiges Spurenelement, häufig nicht ausreichend verfügbar 2+ Verfärbung und Geschmacksbeeinträchtigung ab β(Fe ) = 0,2 mg/L 2+ Gesundheitsschäden erst ab β(Fe ) = 200 mg/L Cu Fe 3+ 2+ 2+ 2+ Für verdünnte Kupfer-Ionen-Lösungen gilt: c(Cu ) = β(Cu ) / (63,5 g/mol) Elektrochemische Spannungsreihe Standardpotentiale in V (c = 1 mol/L, bei = 25 °C und p = 101,3 kPa) 3+ Al/Al 2+ Zn/Zn 2+ Fe/Fe + H2/2 H3O bei pH = 6,8 + H2/2 H3O 2+ Cu/Cu – 4 OH /O2 bei pH = 14 –1,66 –0,76 –0,41 –0,40 0,00 0,35 0,40 Nur für den Dienstgebrauch!

Ministerium für Schule und Weiterbildung NRW CH GK HT 1 Seite 1 von 7 Unterlagen für die Lehrkraft Abiturprüfung 2010 Chemie, Grundkurs 1. Aufgabenart Bearbeitung einer Aufgabe, die auf fachspezifischen Vorgaben basiert 2. Aufgabenstellung Regenwasser vom Kupferdach für den Gartenteich? 1. Erklären Sie die Beobachtungen beim Betrieb der Vorrichtung zum Entkupfern des Regen- wassers. Erklären Sie unter Verwendung entsprechender Fachbegriffe und Reaktions- gleichungen die Funktionsweise dieser Vorrichtung. Prüfen Sie unter Berücksichtigung elektrochemischer und ökologischer Aspekte, ob auch Aluminiumfolie als Füllung für die Vorrichtung zum Entkupfern geeignet ist. (24 Punkte) 2. Geben Sie eine mathematische Beziehung zur Bestimmung der Kupfer-Ionen-Konzen- tration im Wasser an. Berechnen Sie die Spannung der Kupfer-Konzentrationskette für eine Kupfer-Ionen-Konzentration, die empfindliche Fische schädigen kann. Ermitteln Sie, ob das vom Dach ablaufende Regenwasser vor bzw. nach Entkupferung zur Füllung des Gartenteiches geeignet ist. (16 Punkte) 3. Erläutern Sie die Beobachtungen bei Betrieb des elektronischen Gerätes mithilfe von Reaktionsgleichungen. Erläutern Sie, ob die Verwendung von entkupfertem Zisternen- wasser oder der Einsatz eines elektronischen Gerätes hinsichtlich Wirksamkeit und Wartungsaufwand besser zur Algenbekämpfung im Gartenteich geeignet ist. (20 Punkte) 3. Materialgrundlage http://www.dvgw.de/fileadmin/dvgw/wasser/recht/trinkwvo.pdf (23.02.2009) http://www.umweltdaten.de/uba-info-presse/hintergrund/cuzn.pdf (22.02.2009) http://lims.uni-duisburg.de/Tagungen/UAT2000/Abstracts/Untersuchungvon Regenwasser/UntersuchungvonRegenwasser.htm (07.02.2009) http://www.lenntech.com/deutsch/Element-und-Wasser/ (23.02.2009) http://www.velda.de/index.php?id=123&show=100184&lang=de (21.02.2009) Handbook of Chemistry and Physics, 67th Edition, CRC-Press, Boca Taton, Fla. 1986, S. 227 Nur für den Dienstgebrauch!

Ministerium für Schule und Weiterbildung NRW CH GK HT 1 Seite 2 von 7 4. Bezüge zu den Vorgaben 2010 1. Inhaltliche Schwerpunkte Themenfeld: Gewinnung, Speicherung und Nutzung elektrischer Energie in der Chemie Batterien und Akkumulatoren: Grundprinzip der Funktionsweise galvanische Zelle: Vorgänge an Elektroden, Potentialdifferenz Spannungsreihe der Metalle/Nichtmetalle: Additivität der Spannungen, Standardelektrodenpotential Nernst-Gleichung (quantitative Behandlung) – System Metall/Metall-Ion, Systeme Wasserstoff/Oxonium-Ion und Hydroxid-Ion/Sauerstoff (jeweils unter Standardbedingungen) – System Halogenid-Ion/Halogen einfache Elektrolyse im Labor 2. Medien/Materialien entfällt 5. Zugelassene Hilfsmittel Wissenschaftlicher Taschenrechner Periodensystem Wörterbuch zur deutschen Rechtschreibung 6. Vorgaben für die Bewertung der Schülerleistungen Teilleistungen – Kriterien a) inhaltliche Leistung Teilaufgabe 1 Anforderungen Der Prüfling 1 maximal erreichbare Punktzahl (AFB)1 1 erklärt die Beobachtungen beim Betrieb der Vorrichtung zum Entkupfern des Regenwassers, z. B.: Bei dem rötlichen Belag handelt es sich um abgeschiedenes Kupfer. An der Oberfläche der Eisenwolle reagiert das Eisen mit den Kupfer-Ionen. Da hierbei Eisen-Ionen entstehen, löst sich die Eisenwolle mit der Zeit auf. 8 (II) 2 erklärt unter Verwendung entsprechender Fachbegriffe und Reaktionsgleichungen die Funktionsweise der Vorrichtung zum Entkupfern des Regenwassers, z. B.: 2+ 2+ U°(Cu/Cu ) > U°(Fe/Fe ) 2+ – 2+ – Oxidation: Fe Fe + 2e Reduktion: Cu + 2e Cu, 2+ 2+ Gesamtreaktion: Cu + Fe Cu + Fe 8 (I) AFB = Anforderungsbereich Nur für den Dienstgebrauch!

Ministerium für Schule und Weiterbildung NRW CH GK HT 1 Seite 3 von 7 3a prüft unter elektrochemischen Aspekten, ob auch Aluminiumfolie als Füllung für eine Entkupferung geeignet ist. (Hinweis: Es wird erwartet, dass zur Prüfung das Standardpotential von Aluminium herangezogen und Aluminiumfolie als geeignet ermittelt wird.) 4 (I) 3b prüft unter ökologischen Aspekten, ob auch Aluminiumfolie als Füllung für eine Entkupferung geeignet ist. (Hinweis: Es wird erwartet, dass der Prüfling angibt, dass Aluminium-Ionen im Gegensatz zu Eisen-Ionen fischgiftig (bei Konzentrationen über 0,1 mg/L) sind und Aluminium daher als problematischer anzusehen ist.) 4 (I) 4 erfüllt ein weiteres aufgabenbezogenes Kriterium. (2) Teilaufgabe 2 Anforderungen Der Prüfling maximal erreichbare Punktzahl (AFB) 1 gibt eine mathematische Beziehung zur Bestimmung der Kupfer-Ionen-Konzentration im Wasser an, z. B.: 2+ 2+ U(Konzentrationskette) = (59 mV / 2) · lg(c(Cu , Ref.) / c(Cu , Regenwasser)) (Hinweis: Alternativ kann die Differenz der Halbzellenpotentiale gebildet werden.) 2 (I) 2 berechnet die Spannung der Kupfer-Konzentrationskette für eine Kupfer-Ionen- Konzentration, die empfindliche Fische schädigen kann. (Hinweis: Es wird erwartet, dass sich unter Verwendung der Nernst-Gleichung für –6 eine Fische schädigende Konzentration von c = 1,57 · 10 mol/L (β = 0,1 mg/L) eine Spannung von U = 141,7 mV ergibt.) 6 (II) 3a ermittelt, ob das vom Dach ablaufende Regenwasser vor bzw. nach Entkupferung zur Füllung des Gartenteiches geeignet ist, z. B.: 2+ 2+ Berechnung von c(Cu ) und Ermittlung von β(Cu ) 2+ 2+ β(Cu ) = 1,62 mg/L bzw. β(Cu ) = 0,0025 mg/L (Hinweis: Eine Argumentation ausgehend von den Spannungswerten und einem Spannungsvergleich ohne Berechnung der Konzentration wird auch akzeptiert.) 6 (III) 3b ermittelt, ob das vom Dach ablaufende Regenwasser vor bzw. nach Entkupferung zur Füllung des Gartenteiches geeignet ist, indem er z. B. darstellt, dass entkupfertes Regenwasser im Gegensatz zu nicht entkupfertem Regenwasser zur Füllung des Gartenteiches geeignet ist, da die Kupfer-Ionen-Konzentration unter dem Grenzwert liegt, bei dem Fische geschädigt werden können, aber über dem Grenzwert, bei dem Algen geschädigt werden. 2 (II) 4 erfüllt ein weiteres aufgabenbezogenes Kriterium. (2) Nur für den Dienstgebrauch!

Ministerium für Schule und Weiterbildung NRW CH GK HT 1 Seite 4 von 7 Teilaufgabe 3 Anforderungen Der Prüfling 1 erläutert die Beobachtungen bei Betrieb des elektronischen Gerätes mithilfe von Reaktionsgleichungen, z. B.: 2+ – Anode: Cu Cu + 2e , die Kupfer-Ionen-Konzentration nimmt folglich zu. + – Kathode: 2 H + 2e H2 (g), es bildet sich daher ein Gas. maximal erreichbare Punktzahl (AFB) 6 (II) 2a erläutert, ob die Verwendung von entkupfertem Zisternenwasser oder der Einsatz 8 (III) eines elektronischen Gerätes hinsichtlich Wirksamkeit und Wartungsaufwand besser zur Algenbekämpfung geeignet ist, z. B.: Beide Methoden erzeugen eine Kupfer-Ionen-Konzentration, die zur Algen- bekämpfung geeignet ist. Das elektronische Gerät erzeugt eine Kupfer-Ionen-Konzentration, bei der emp- findliche Fische geschädigt werden können; bei der Entkupferungsvorrichtung wird eine Fische schädigende Kupfer-Ionen-Konzentration nur dann erreicht, wenn nicht mehr ausreichend Eisenwolle vorhanden ist. Bei Haltung empfindlicher Fische ist der Einsatz von entkupfertem Regenwasser vorzuziehen. Ansonsten wäre das elektronische Gerät vorzuziehen, da es wegen der höheren Kupfer-Ionen-Konzentration wirksamer gegen Algen ist. 2b erläutert, ob die Verwendung von entkupfertem Zisternenwasser oder der Einsatz eines elektronischen Gerätes hinsichtlich Wirksamkeit und Wartungsaufwand besser zur Algenbekämpfung geeignet ist, indem er Vorzüge bzw. Nachteile wie z. B. Aus- tausch der Kupfer-Anode bzw. Ersatz der Eisenwolle darstellt. 3 6 (II) erfüllt ein weiteres aufgabenbezogenes Kriterium. (2) b) Darstellungsleistung Anforderungen Der Prüfling maximal erreichbare Punktzahl 1 führt seine Gedanken schlüssig, stringent und klar aus. 4 2 3 strukturiert seine Darstellung sachgerecht und übersichtlich, verwendet eine differenzierte und präzise Sprache, veranschaulicht seine Ausführungen durch geeignete Skizzen, Schemata etc., gestaltet seine Arbeit formal ansprechend. Nur für den Dienstgebrauch!

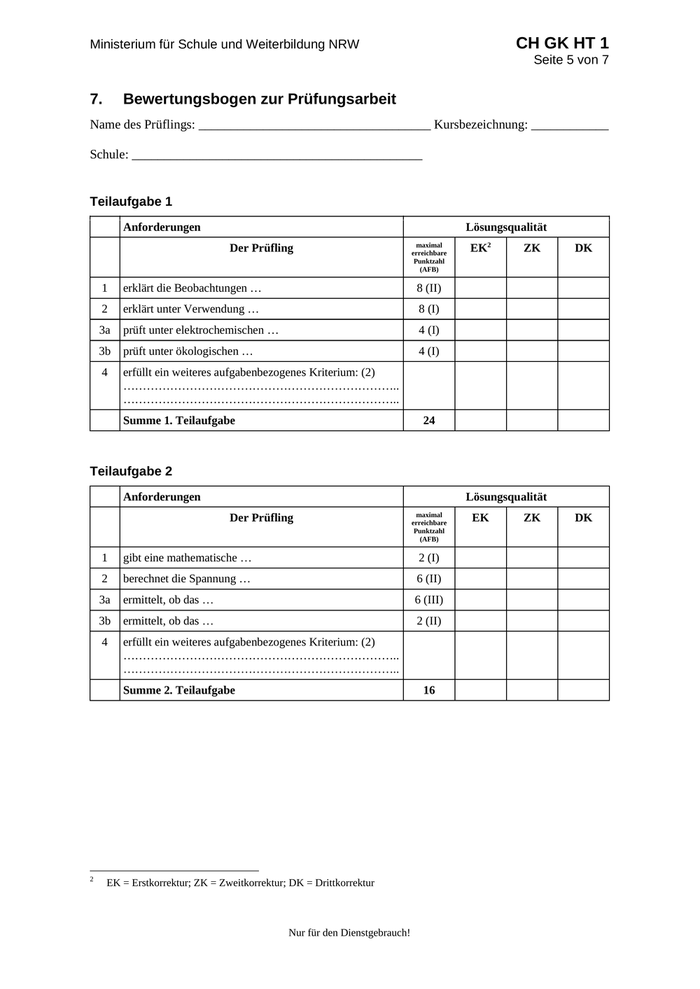
CH GK HT 1 Ministerium für Schule und Weiterbildung NRW Seite 5 von 7 7. Bewertungsbogen zur Prüfungsarbeit Name des Prüflings: ____________________________________ Kursbezeichnung: ____________ Schule: _____________________________________________ Teilaufgabe 1 Anforderungen Lösungsqualität Der Prüfling maximal erreichbare Punktzahl (AFB) 1 erklärt die Beobachtungen … 8 (II) 2 erklärt unter Verwendung … 8 (I) 3a prüft unter elektrochemischen … 4 (I) 3b prüft unter ökologischen … 4 (I) 4 erfüllt ein weiteres aufgabenbezogenes Kriterium: (2) …………………………………………………………….. …………………………………………………………….. Summe 1. Teilaufgabe EK 2 ZK DK 24 Teilaufgabe 2 Anforderungen Lösungsqualität Der Prüfling 1 gibt eine mathematische … 2 (I) 2 berechnet die Spannung … 6 (II) 3a ermittelt, ob das … 6 (III) 3b ermittelt, ob das … 2 (II) 4 erfüllt ein weiteres aufgabenbezogenes Kriterium: (2) …………………………………………………………….. …………………………………………………………….. Summe 2. Teilaufgabe 2 maximal erreichbare Punktzahl (AFB) 16 EK = Erstkorrektur; ZK = Zweitkorrektur; DK = Drittkorrektur Nur für den Dienstgebrauch! EK ZK DK
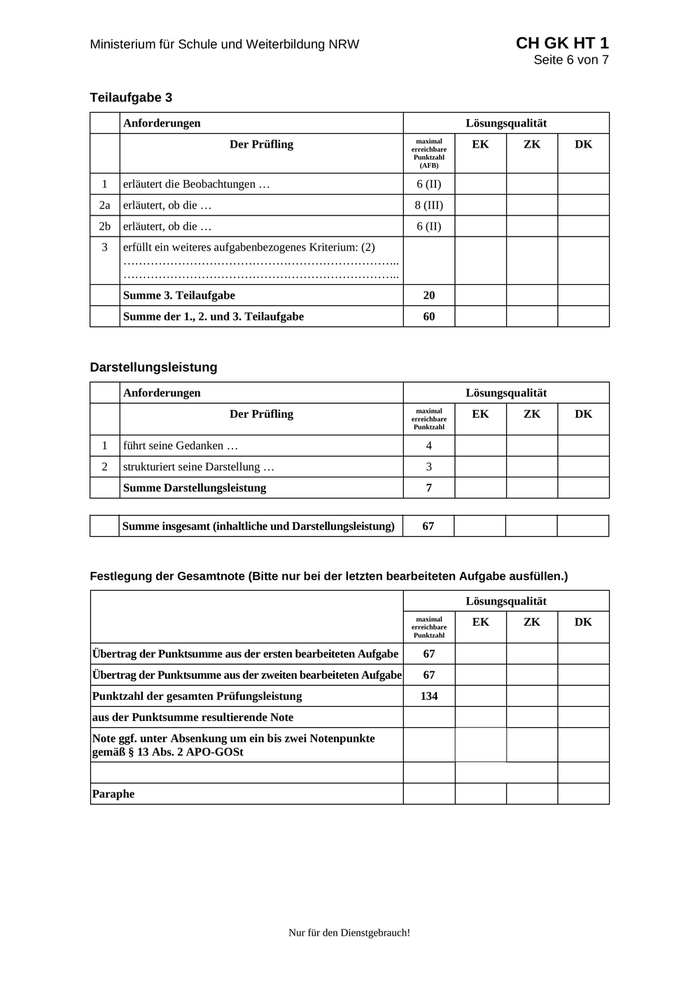
CH GK HT 1 Ministerium für Schule und Weiterbildung NRW Seite 6 von 7 Teilaufgabe 3 Anforderungen Lösungsqualität Der Prüfling maximal erreichbare Punktzahl (AFB) 1 erläutert die Beobachtungen … 6 (II) 2a erläutert, ob die … 8 (III) 2b erläutert, ob die … 6 (II) 3 erfüllt ein weiteres aufgabenbezogenes Kriterium: (2) …………………………………………………………….. …………………………………………………………….. Summe 3. Teilaufgabe 20 Summe der 1., 2. und 3. Teilaufgabe 60 EK ZK DK Darstellungsleistung Anforderungen Lösungsqualität Der Prüfling maximal erreichbare Punktzahl 1 führt seine Gedanken … 4 2 strukturiert seine Darstellung … 3 Summe Darstellungsleistung 7 Summe insgesamt (inhaltliche und Darstellungsleistung) EK ZK DK 67 Festlegung der Gesamtnote (Bitte nur bei der letzten bearbeiteten Aufgabe ausfüllen.) Lösungsqualität maximal erreichbare Punktzahl Übertrag der Punktsumme aus der ersten bearbeiteten Aufgabe 67 Übertrag der Punktsumme aus der zweiten bearbeiteten Aufgabe 67 Punktzahl der gesamten Prüfungsleistung 134 aus der Punktsumme resultierende Note Note ggf. unter Absenkung um ein bis zwei Notenpunkte gemäß § 13 Abs. 2 APO-GOSt Paraphe Nur für den Dienstgebrauch! EK ZK DK
CH GK HT 1 Ministerium für Schule und Weiterbildung NRW Seite 7 von 7 ggf. arithmetisches Mittel der Punktsummen aus EK und ZK: ___________ ggf. arithmetisches Mittel der Notenurteile aus EK und ZK: _____________ Die Klausur wird abschließend mit der Note: ________________________ (____ Punkte) bewertet. Unterschrift, Datum: Grundsätze für die Bewertung (Notenfindung) Für die Zuordnung der Notenstufen zu den Punktzahlen ist folgende Tabelle zu verwenden: Note Punkte Erreichte Punktzahl sehr gut plus 15 134 – 128 sehr gut 14 127 – 121 sehr gut minus 13 120 – 114 gut plus 12 113 – 108 gut 11 107 – 101 gut minus 10 100 – 94 befriedigend plus 9 93 – 87 befriedigend 8 86 – 81 befriedigend minus 7 80 – 74 ausreichend plus 6 73 – 67 ausreichend 5 66 – 61 ausreichend minus 4 60 – 52 mangelhaft plus 3 51 – 44 mangelhaft 2 43 – 36 mangelhaft minus 1 35 – 27 ungenügend 0 26 – 0 Nur für den Dienstgebrauch!










