204c-bntcom01634-p21285-flyer-stabilitaetsdaten-comirnaty-5-11y-211209-002
Dieses Dokument ist Teil der Anfrage „Briefverkehr mit BioNtech“
COVID-19-mRNA-Impfstoff COMIRNATY ®
Stabilitätsdaten
Stand: 26.11.2021
WICHTIG: Bitte prüfen Sie regelmäßig, ob Ihnen
die aktuellen Stabilitätsdaten der jeweiligen
Darreichungsformen von COMIRNATY® vorliegen:
haltbarkeit.biontech.de
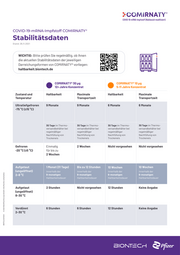
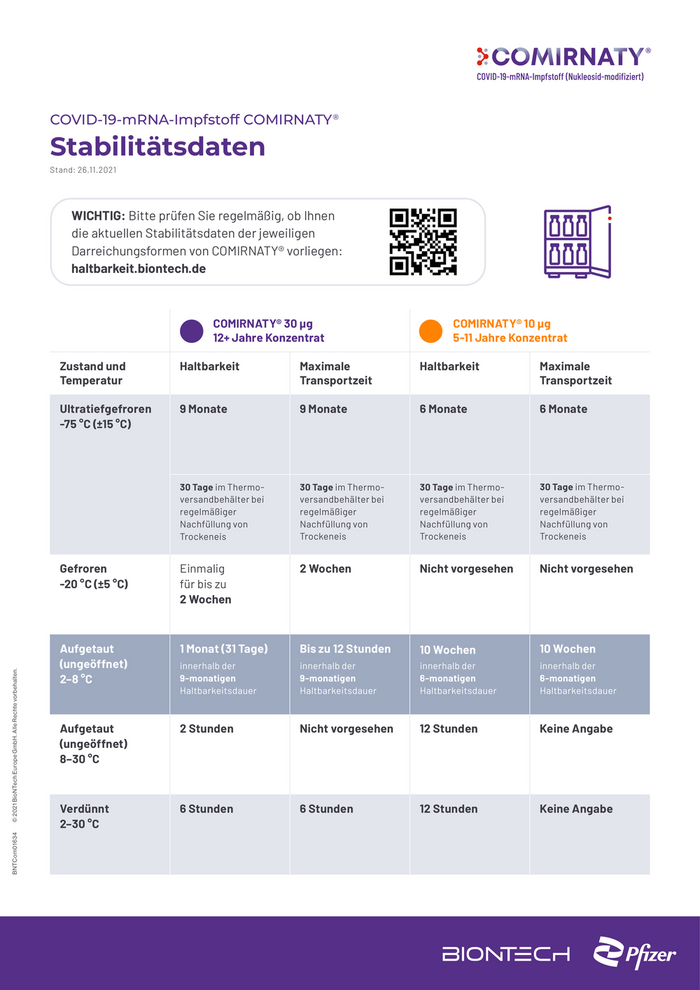
COMIRNATY® 30 µg COMIRNATY® 10 µg
12+ Jahre Konzentrat 5-11 Jahre Konzentrat
Zustand und Haltbarkeit Maximale Haltbarkeit Maximale
Temperatur Transportzeit Transportzeit
Ultratiefgefroren 9 Monate 9 Monate 6 Monate 6 Monate
-75 °C (±15 °C)
30 Tage im Thermo- 30 Tage im Thermo- 30 Tage im Thermo- 30 Tage im Thermo-
versandbehälter bei versandbehälter bei versandbehälter bei versandbehälter bei
regelmäßiger regelmäßiger regelmäßiger regelmäßiger
Nachfüllung von Nachfüllung von Nachfüllung von Nachfüllung von
Trockeneis Trockeneis Trockeneis Trockeneis
Gefroren Einmalig 2 Wochen Nicht vorgesehen Nicht vorgesehen
-20 °C (±5 °C) für bis zu
2 Wochen
Aufgetaut 1 Monat (31 Tage) Bis zu 12 Stunden 10 Wochen 10 Wochen
(ungeöffnet) innerhalb der innerhalb der innerhalb der innerhalb der
© 2021 BioNTech Europe GmbH. Alle Rechte vorbehalten.
2–8 °C 9-monatigen 9-monatigen 6-monatigen 6-monatigen
Haltbarkeitsdauer Haltbarkeitsdauer Haltbarkeitsdauer Haltbarkeitsdauer
Aufgetaut 2 Stunden Nicht vorgesehen 12 Stunden Keine Angabe
(ungeöffnet)
8–30 °C
Verdünnt 6 Stunden 6 Stunden 12 Stunden Keine Angabe
2–30 °C
BNTCom01634
COVID-19-mRNA-Impfstoff COMIRNATY ®
Wichtige Stabilitätshinweise
Bitte beachten Sie die Hinweise zu den Stabilitätsdaten der jeweiligen Darreichungsform des Impfstoffs.
Es ist wichtig, die Vorgaben zu Kühlung, Transport und Haltbarkeit genau einzuhalten. Die aktuellen Stabilitäts-
daten der jeweiligen Darreichungsformen finden Sie unter: haltbarkeit.biontech.de
Nach Entnahme des gefrorenen Impfstoffs aus der Ultratiefkühlung (zum Beispiel
zum Transfer vom Thermoversandbehälter in den Ultra-Tieftemperatur-Gefrier-
schrank) muss der Impfstoff mindestens 2 Stunden in der Ultratiefkühlung ver-
bleiben, bevor er erneut entnommen werden darf.
Der gefrorene Impfstoff sollte in der Faltschachtel im Kühlschrank bei 2 bis 8 °C
über einen Zeitraum von 3 bis 4 Stunden auftauen. Alternativ können einzelne
gefrorene Durchstechflaschen zur sofortigen Verwendung auch 30 Minuten lang
bei Temperaturen bis zu 30 °C aufgetaut werden.
Stellen Sie sicher, dass die Durchstechflaschen vor der Verwendung vollständig
aufgetaut sind.
Einmal aufgetaute Durchstechflaschen dürfen nicht wieder eingefroren werden.
Bitte achten Sie auf die Transportzeiten gemäß den aktuellen Stabilitätsdaten
der jeweiligen Darreichungsformen. Die verdünnte Dispersion nicht einfrieren
oder schütteln.
© 2021 BioNTech Europe GmbH. Alle Rechte vorbehalten.
Längere Haltbarkeit: Bitte beachten Sie die Hinweise für die
erweiterte Lagerungsdauer bereits im Umlauf befindlicher Chargen
von COMIRNATY® 30 µg 12+ Jahre Konzentrat auf Seite 3.
BNTCom01634

COVID-19-mRNA-Impfstoff COMIRNATY ®
Wichtige Stabilitätshinweise
Längere Haltbarkeit bereits im Umlauf befindlicher
Chargen von COMIRNATY® 30 µg 12+ Jahre Konzentrat
Die Haltbarkeit der ungeöffneten und bei -75 °C (±15 °C) tiefgefrorenen Durchstechflaschen
von COMIRNATY® 30 µg 12+ Jahre Konzentrat hat sich im September 2021 von 6 auf 9 Monate
verlängert. Dies gilt auch für bereits im Umlauf befindliche Chargen.
Durchstechflaschen mit einem auf dem Etikett aufgedruckten Verfallsdatum von Oktober 2021
bis März 2022 können noch 3 Monate über das aufgedruckte Datum hinaus verwendet werden,
sofern diese bei -75 °C (±15 °C) gelagert werden:
Aufgedrucktes Verfallsdatum Neues Verfallsdatum
Oktober 2021 Januar 2022
November 2021 Februar 2022
Dezember 2021 März 2022
Januar 2022 April 2022
Februar 2022 Mai 2022
März 2022 Juni 2022
Alle Durchstechflaschen von COMIRNATY® 30 µg 12+ Jahre Konzentrat mit einem Verfallsdatum
nach März 2022 weisen bereits die 9-monatige Haltbarkeitsdauer auf.
© 2021 BioNTech Europe GmbH. Alle Rechte vorbehalten.
Wichtig: Die neue Formulierung COMIRNATY® 10 µg 5-11 Jahre
Konzentrat hat bei -75 °C (±15 °C) eine Haltbarkeit von 6 Monaten.
Fachinformation BioNTech Kundenservice
Alle Produktmerkmale Tel: +49 6131 9084-0, Fax: -2121
und Anwendungshinweise E-Mail: service@biontech.de
BNTCom01634
finden Sie unter: (täglich: 08:00–22:00 Uhr)
fachinformation.biontech.de service.biontech.de

Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung
© 2021 BioNTech Europe GmbH. Alle Rechte vorbehalten.
COMIRNATY® Wirkstoff: Tozinameran, COVID-19-mRNA-Impfstoff.
COMIRNATY® 30 Mikrogramm/Dosis Konzentrat zur Herstellung einer Injektionsdispersion (ab 12 Jahre): Zusammensetzung: Nach der Verdünnung enthält die Durchstechflasche 6 Dosen von 0,3 ml mit
jeweils 30 Mikrogramm mRNA. Sonstige Bestandteile: ((4-Hydroxybutyl)azandiyl)bis(hexan-6,1-diyl)bis(2-hexyldecanoat) (ALC-0315), 2-[(Polyethylenglykol)-2000]-N,N-ditetradecylacetamid (ALC-0159),
Colfoscerilstearat (DSPC), Cholesterol, Kaliumchlorid, Kaliumdihydrogenphosphat, Natriumchlorid, Natriummonohydrogenphosphat Dihydrat, Sucrose, Wasser für Injektionszwecke, Natriumhydroxid
(zur pH-Einstellung), Salzsäure (zur pH-Einstellung) COMIRNATY® 30 Mikrogramm/Dosis Injektionsdispersion (ab 12 Jahre): Zusammensetzung: Wirkstoff: Tozinameran, COVID-19-mRNA-Impfstoff. Eine
Durchstechflasche enthält 6 Dosen von 0,3 ml mit jeweils 30 Mikrogramm mRNA. Sonstige Bestandteile: ((4-Hydroxybutyl)azandiyl)bis(hexan-6,1-diyl)bis(2-hexyldecanoat) (ALC-0315), 2-[(Polyethylenglykol)-
2000]-N,N-ditetradecylacetamid (ALC-0159), Colfoscerilstearat (DSPC), Cholesterol, Trometamol, Trometamolhydrochlorid, Sucrose, Wasser für Injektionszwecke. COMIRNATY® 10 Mikrogramm/Dosis
Konzentrat (5-11 Jahre): Zusammensetzung: Eine Durchstechflasche enthält 10 Dosen von 0,2 ml mit jeweils 10 Mikrogramm mRNA. Sonstige Bestandteile: ((4-Hydroxybutyl)azandiyl)bis(hexan-6,1-diyl)
bis(2-hexyldecanoat) (ALC-0315), 2-[(Polyethylenglykol)-2000]-N,N-ditetradecylacetamid (ALC-0159), Colfoscerilstearat (DSPC), Cholesterol, Trometamol, Trometamolhydrochlorid, Sucrose, Wasser für
Injektionszwecke. Anwendungsgebiete: Aktive Immunisierung zur Vorbeugung von COVID-19 durch das SARS-CoV-2-Virus bei Kindern im Alter von 5 bis 11 Jahren (Dosis 10 Mikrogramm in 0,2ml) bzw. Personen
ab 12 Jahren (Dosis 30 Mikrogramm in 0,3ml). Gegenanzeigen: Allergie gegen einen der Bestandteile des Arzneimittels. Nebenwirkungen: Sehr häufig: Schmerzen, Schwellung, Rötung (bei 5-11-jährigen
Kindern) an der Injektionsstelle; Ermüdung; Kopfschmerzen; Muskelschmerzen; Schüttelfrost, Gelenkschmerzen; Durchfall, Fieber. Häufig: Rötung an der Injektionsstelle; Übelkeit, Erbrechen. Gelegentlich:
vergrößerte Lymphknoten (häufiger beobachtet nach der Auffrischungsdosis); Unwohlsein; Armschmerzen; Schlaflosigkeit; Jucken an der Injektionsstelle, allergische Reaktionen wie Ausschlag oder
Juckreiz; Schwächegefühl oder Energiemangel/Schläfrigkeit, verminderter Appetit, starkes Schwitzen, nächtliche Schweißausbrüche. Selten: vorübergehendes, einseitiges Herabhängen des Gesichtes;
allergische Reaktionen wie Nesselsucht oder Schwellung des Gesichts. Häufigkeit nicht bekannt: schwere allergische Reaktionen; Entzündung des Herzmuskels (Myokarditis) oder Entzündung des Herzbeutels
(Perikarditis), die zu Atemnot, Herzklopfen oder Schmerzen in der Brust führen können; ausgedehnte Schwellung der geimpften Gliedmaße; Anschwellen des Gesichts (ein geschwollenes Gesicht kann bei
Patienten auftreten, denen in der Vergangenheit dermatologische Filler im Gesichtsbereich injiziert wurden); eine Hautreaktion, die rote Flecken oder Stellen auf der Haut verursacht, die wie ein Ziel oder eine
BNTCom01634
Zielscheibenmitte mit einer dunkelroten Mitte aussehen können, das von hellroten Ringen umgeben ist (Erythema multiforme).
Verschreibungspflichtig. Stand der Informationen: 26. November 2021. Pharmazeutischer Unternehmer: BioNTech Manufacturing GmbH, An der Goldgrube 12, 55131 Mainz.
Weitere Informationen, Warnhinweise und Vorsichtsmaßnahmen sind der Fachinformation zu entnehmen. www.comirnatyglobal.com.