bfr-chlorpyrifos-f.pdf
Dieses Dokument ist Teil der Anfrage „Gutachten zu Chlorpyrifos“
t) Seite 1 von 10 I 6-6212-o4-10241oo3 Anlage 20.11.2018 Gesundheitliche Bewertung der Überschreitung der Rückstandshöchstgehalte von Carbendazim, Chlorpyrifos, lambda-Cyhalothrin, Dimethoat und Omethoat in Guaven 1. Gegenstand der Bewertung Das Bundesinstitut für Risikobewertung (BfR) wurde mit Schreiben des Bundesministeriums für Ernährung und Landwirtschaft (Referat 313) vom 12. November 2018 um Stellungnahme zu einer Anfrage des Hessischen Ministeriums für Umwelt, Klimaschutz, Landwirtschaft und Verbraucherschutz, Referat V2 "Lebensmittel pflanzlicher Herkunft, Bedarfsgegenstände, Weinkontrolle , LHL" gebeten . ln der Anfrage wird um eine gesundheitliche Risikobewertung zu drei Proben von Guaven aus Ägypten gebeten, in denen folgende Rückstände nachgewiesen wurden. Probennummer 1 2 3 2. Nachgewiesene Rückstände (mg/kg) 0,3 mg/kg Carbendazim 0,17 mg/kg Chlorpyriphos 0,06 mg/kg lambda-Cyhaloth ri n 0,026 mg/kg Dimethoat 0,043 mg/kg Omethoat 0,023 mg/kg Dimethoat Ergebnis Für die toxikolog ische Bewertung liegen für alle in den Guaven-Proben nachgewiesenen Wirkstoffe toxikologische Grenzwerte aus dem EU-Verfahren zur Genehmigung von Pflanzenschutzmitlei-Wirkstoffen vor. Die gesundheitliche Risikobewertung des in Guaven ermittelten Rü ckstandbefundes erfolgte auf Basis deutscher und europäischer Verzehrsdaten . Da Guaven ein selten verzehrtes Lebensmittel in Europa darstellen , sind diese Daten jedoch nicht ausreichend robust für eine alleinige Expositionsschätzung . Daher wurden diese Daten mit Verzehrsdaten für Erwachsene aus Brasilien ergänzt, die wahrscheinlich im Verg leich zum europäischen Ernährungsverhalten für Guave einen kritischeren Fall darstellen . Für Probe 1 wurden die individuellen ARfD der nachgewiesenen Einzelverbindungen Carbendazim (bis zu 40 % der ARfD von 0,02 mg/kg KG) , Chlorpyrifos (bis zu 100 % der ARfD von 0,005 mg/kg KG) und lambda-Cyhalothrin (bis zu 30 % der ARfD von 0,005 mg/kg KG) auf Basis deutscher, europäischer und brasilianischer Verzehrsdaten für Guave nicht überschritten . Eine gesundheitliche Beeinträchtigung durch die Einzelstoffe wird praktisch ausgeschlossen. Ergänzend wurde jedoch festgestellt, dass in Probe 1 zwei Wirkstoffe mit neurotoxischem Potential nachgewiesen wurden , für welche eine add itive Wirk ung zum gegenwärtigen

Seite 2 von 10 Zeitpunkt nicht ausgeschlossen werden kann. Die kumulative Bewertung ergab einen Hazard Index (HI) von 1,01 für Kinder aus den Niederlanden sowie von 1,3 für Erwachsene auf Basis der brasilianischen Verzehrsdaten. Da der Hl einen Wert von 1,0 überschreitet, wenn auch nur in geringem Maße, ist ein kumulatives gesundheitliches Risiko durch Probe 1 grundsätzlich möglich. Als gesundheitliche Beeinträchtigung sind reversible klinische Symptome wie vermehrte Speichelbildung und Tränenfluss, Kopfschmerzen, Schwindel- und Schwächegefühl als Folge einer Hemmung der Cholinesterase-Aktivität durch Chlorpyrifos, in Betracht zu ziehen. Lambda-Cyhalothrin blockiert die spannungsabhängigen Natriumkanäle an den Nervenbahnen und folgende reversible klinische Symptome werden berichtet: Reizungen und Rötungen der Haut und Schleimhaut, Kribbeln und Jucken, Augenbrennen, Atemwegsreizungen, Übelkelt und Erbrechen. ln Probe 2 und 3 wurden ausschließlich Rückstände der Wirkstoffe Dimethoat und seines Abbauprodukts Omethoat nachgewiesen. Die Bewertung dieser Rückstände erfolgte auf Basis einer ARfD von 0,01 mg/kg KG für Dimethoat und unter Berücksichtigung eines toxikologischen Äquivalenzfaktors von 6 für akute Effekte von Omethoat. Die Abschätzung der akuten Exposition auf Basis deutscher, europäischer und brasilianischer Verzehrsdaten für Guave ergibt keine Überschreitung der ARfD für Kinder oder Erwachsene durch die Proben 2 und 3. Eine akute Gesundheitsgefährdung durch diese Proben ist praktisch ausgeschlossen. 3. Begründung I Risikobewertung 3.1 Toxikologische Bewertung der Wirkstoffe 3.1.1 Carbendazim Der Wirkstoff Carbendazim ist als genatoxisch (aneugene Wirkung mit Schwellenwert) und reproduktionstoxisch eingestuft (Kategorie 1B, Verordnung (EG) Nr. 1272/2008). Der Wirkstoff ist seit 2014 in der EU nicht mehr als Pflanzenschutzmittel-Wirkstoft genehmigt. Die nachfolgende Tabelle fasst die früheren im EU-Verfahren abgeleiteten toxikologischen Grenzwerte für Carbendazim zusammen. Abgeleitete toxikologische Grenzwerte für Carbendazim Bezeichnung Wert StUdie !Tierart Sicherheits- faktor Quelle ADI 0.02 Entwicklungstoxizität/ Ratte und Kaninchen 500 EFSA Journal 2010; 8(5): 1598 ARfD 0.02 Entwicklungstoxizität/ Ratte und Kaninchen 500 EFSA Journal 2010; 8(5): 1598 3.1.2 Chlorpyrites Chlorpyrifos ist bis zum 31.01.2019 in der EU als Pflanzenschutzmittel-Wirkstoft genehmigt.

Seite 3 von 10 Der Wirkstoff Chlorpyrifos wurde nach den heute üblichen Anforderungen toxikologisch untersucht (EFSA Journal 2014;12(4):3640). Die Daten sind ausreichend, um die möglichen Gefahren für die Gesundheit bewerten zu können. Die nachfolgende Tabelle fasst die Grenzwerte für Chlorpyrifos zusammen. im EU-Verfahren abgeleiteten toxikologischen Toxikologische Grenzwerte für Chlorpyrites Bezeichnung Wert Studie !Tierart Sicherheits- faktor Quelle ADI 0,001 mg/kg KG/d 2-Jahresstudien, Ratte und Hund 100 ARfD 0,005 mg/kg KG Akute Neurotoxizität (Acetylcholinesterase- Hemmung), Ratte 100 EFSA Journal 2014;12(4):3 1 640 3.1.3 Lambda-Cyhalothrin Lambda-Cyhalothrin ist bis zum 31.03.2023 in der EU als Pflanzenschutzmittel-Wirkstoft genehmigt. Während des EU-Bewertungsprozesses wurden eine Reihe fehlender Informationen identifiziert, z. 8. toxikologische Daten zu Metaboliten und Effekten auf die Spermatogenese (EFSA Journal 2014;12(5):3677), die im gegenwärtigen ,Post approvai- Verfahren' vorgelegt wurden. Die abschließende EU-Bewertung der nachgereichten Daten steht noch aus. Die nachfolgende Tabelle fasst die im EU-Verfahren Grenzwerte für lambda-Cyhalothrin zusammen. abgeleiteten toxikologischen Toxikologische Grenzwerte für lambda-Cyhalothrin 1 Bezeichnung Wert Studie !Tierart Sicherheits- faktor Quelle ADI 0,0025 mg/kg KG Multigenerationsstudie, (Cyhalothrin), Ratte 200 ARfD 0,005 mglkg KG 1-Jahresstudie, Hund (klinische Zeichen für Neurotoxizität) 100 EFSA Journal 2014;12(5):3 677 EFSA Journal 2014; 12(4):3640 Conclusion on the peer review of the pesticide human health risk assessment of the active substance chlorpyrifos

Seite 4 von 10 3.1.4 Dimethoat (einschließlich Omethoat) Omethoat ist in der EU nicht als Pflanzenschutzmitlei-Wirkstoff genehmigt. Omethoat entsteht jedoch auch als Hauptmetabolit des Pflanzenschutzmittei-Wirkstoffs Dimethoat, der bis zum 31.07.2019 in der EU als Wirkstoff genehmigt ist. Der Wirkstoff Dimethoat wurde nach den heute üblichen Anforderungen toxikologisch untersucht (EFSA Journal 2013; 11 (7):3233, RAR 2017). Die Daten sind ausreichend, um die möglichen Gefahren für die Gesundheit bewerten zu können. Die nachfolgende Tabelle fasst die im EU-Verfahren abgeleiteten toxikologischen Grenzwerte für Dimethoat zusammen. Aufgrund der qualitativ vergleichbaren Wirkung von Dimethoat und Omethoat können die toxikologischen Grenzwerte von Dimethoat auch zur Bewertung von Omethoat verwendet werden, sofern dabei die unterschiedliche Wirkstärke berücksichtigt wird. Im EU-Verfahren wurden dafür die Faktoren 3 (chronische Exposition) und 6 (akute Exposition) verwendet, die sich aus den entsprechenden NOAELs ableiten 2 lassen . Toxikologische Grenzwerte für Dimethoat Bezeichnung Wert Studie merart Sicherheits- faktor Quelle ADI 0,001 mg/kg KG Multigenerationsstudie, subchronische Neurotoxizitätsstudie, Entwicklungs- Neurotoxitätsstudie, Ratte 100 EFSA Journal 2013;11(7):3 3 233 , RAR 2017 ARfD 0,01 mg/kg KG Akute Neurotoxizität, Ratte 100 Zu weiteren Ausführungen wird auf die Stellungnahme des BfR aus dem Juni 2013 verwiesen (BfR-Stellungnahme 6-6212-04-7378530). 3.2 Abschätzung der Kurzzeit-Aufnahmemenge (IESTI) Guave stellt ein in Europa selten verzehrtes Lebensmittel dar, für das nur bedingt 4 repräsentative Verzehrdaten vorliegen. Sowohl im deutschen NVS II-Modell für Kinder und 5 Erwachsene als auch im EFSA-PRIMo-Modell (Version 3) konnten daher verlässliche 97,5te Perzentile für die Portionsgröße zur Ermittlung der Kurzzeit-Aufnahmemenge nicht abgeleitet werden. Es wurde in beiden Modellen auf das Maximum bzw. einen Schätzwert 6 zurückgegriffen. Aus dem IESTI-Modell der FAO/WH0 stehen Verzehrmengen von Guave 2 EFSA Scientific Report (2006) 84, 1-102, Conclusion on the peer review of dimethoate (23.06.2007) 3 EFSA Journal 2013; 11 (7):3233 Peer Review of the pesticide risk assessment of confirmatory data submitted for the active substance dimethoate 4 http://www.bfr.bund.de/cm/343/bfr-berechnungsmodell-zur-aufnahme-von-pflanzenschutzmittel- rueckstaenden-nvs2.zip 5 https://www.efsa.europa.eu/sites/default/files/applications/EFSA PRIMo rev3.xlsm 6 https://www.who.int/foodsafety/areas work/chemical-risks!IESTI calculation 18 model final.xlsm V

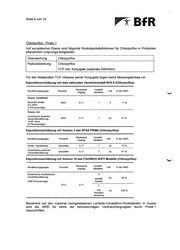
Seite 5 von 10 für Erwachsene aus Brasilien zur Verfügung, die wahrscheinlich im Vergleich zum europäischen Ernährungsverhalten für Guave einen kritischeren Fall darstellen. Für die · Bewertung akuter gesundheitlicher Risiken werden alle drei zur Verfügung stehenden Modelle parallel berücksichtigt. Carbendazim - Probe 1 Auf europäischer Ebene sind folgende Rückstandsdefinitionen für Carbendazim in Produkten pflanzlichen Ursprungs festgesetzt: Überwachung Carbendazim Risikobewertung Carbendazim Expositionsschätzung mit dem nationalen Verzehrsmodell NVS II (Carbendazim) Bevölkerungsgruppe Perzentil Rückstand (mg/kg) Variabili- tätsfaktor Fall %derARfD Guave, verarbeitet deutsche Kinder. 2-4 Jahre (3 Personentage) MAX 0,3 MAX 0,3 3 <1% 2a 18% Guave, roh erwachsene deutsche Gesamtbevölkerung, 14-80 Jahre (2 Personentage) 7 Expositionsschätzung mit Version 3 des EFSA PRIMo (Carbendazim) Bevölkerungsgruppe Perzentil Rückstand (mg/kg) Variabili- tätsfaktor Kinder. Niederlande Geschätzt 0,3 7 2a 33% erwachsene polnische Gesamtbevölkerung Geschätzt 0,3 7 2a 27% Fall % derARfD Expositionsschätzung mit Version 18 des FAO/WHO IESTI Modells (Carbendazim) Bevölkerungsgruppe Perzentil Rückstand (mg/kg) erwachsene brasilianische Gesamtbevölkerung Variabili- tätsfaktor Fall % derARfD 3 (Modell- basiert) (398 Personentage) 97,5 0,3 2a 30% 2a 40% 7 (EU Standard- annahme) Basierend auf den maximal nachgewiesenen Carbendazim-Rückständen in Guave wird die ARfD für keine der berücksichtigten Verbrauchergruppen durch Probe 1 überschritten.
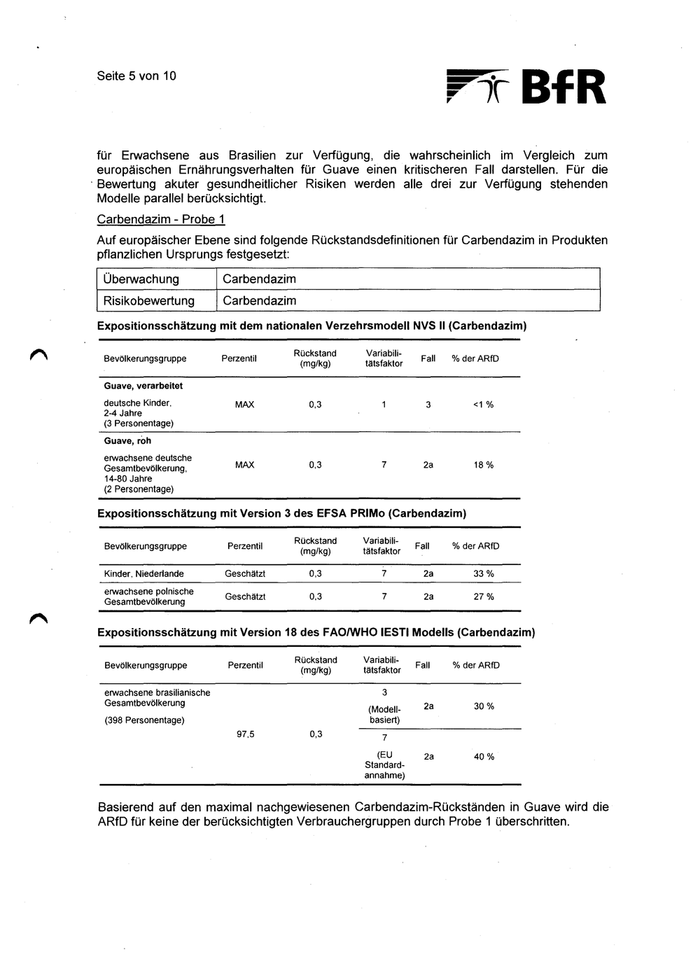
~ir Seite 6 von 10 BfR Chlorpyrifos - Probe 1 Auf europäischer Ebene sind folgende Rückstandsdefinitionen für Chlorpyrifos in Produkten pflanzlichen Ursprungs festgesetzt: Überwachung Chlorpyrifos Risikobewertung Chlorpyrifos TCP inkl. Konjugate (separate Definition) Für den Metaboliten TCP inklusive seiner Konjugate liegen keine Messergebnisse vor. Expositionsschätzung mit dem nationalen Verzehrsmodell NVS II (Chlorpyrifos) Bevölkerungsgruppe Perzentil Rückstand (mg/kg) Variabili- tätsfaktor Fall % derARID Guave, verarbeitet deutsche Kinder, 2-4 Jahre (3 Personentage) MAX 0,17 MAX 0,17 3 <1% 2a 41% Guave, roh erwachsene deutsche Gesamtbevölkerung, 14-80 Jahre (2 Personentage) 7 Expositionsschätzung mit Version 3 des EFSA PRIMo (Chlorpyrifos) Bevölkerungsgruppe Perzentil Rückstand (mg/kg) Variabili- tätsfaktor Kinder, Niederlande Geschatzt 0,17 7 2a 75% erwachsene polnische Gesamtbevölkerung Geschlitzt 0,17 7 2a 61% Fall % derARID Expositionsschätzung mit Version 18 des FAO/WHO IESTI Modells (Chlorpyrifos) Bevölkerungsgruppe Perzentil Rückstand (mg/kg) Erwachsene brasilianische Gesamtbevölkerung Variabili- tätsfaktor Fall %der ARID 3 (Modell- basiert) (398 Personentage) 97,5 0,17 2a 60% 2a 100% 7 (EU Standard- annahme) Basierend auf den maximal nachgewiesenen Lambda-Cyhalothrin-Rückständen in Guave wird die ARfD für keine der berücksichtigen Verbrauchergruppen durch Probe 1 überschritten. V
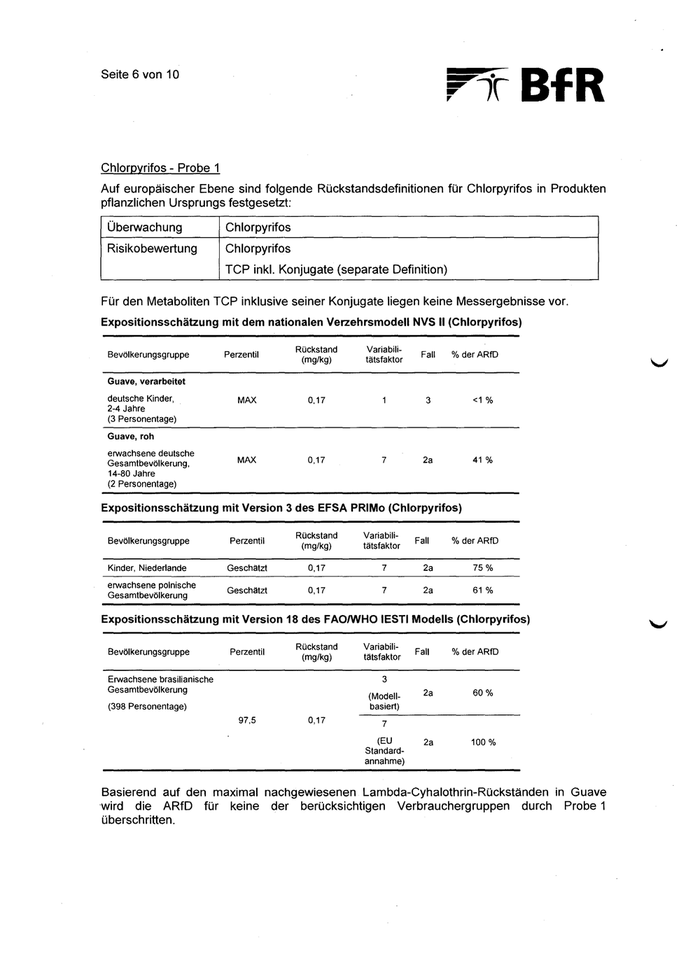
Seite 7 von 10 Lambda-Cyhalothrin - Probe 1 Auf europäischer Ebene sind folgende Rückstandsdefinitionen für Lambda-Cyhalothrin in Produkten pflanzlichen Ursprungs festgesetzt: Überwachung Lambda-Cyhalothrin Risikobewertung Lambda-Cyhalothrin Expositionsschätzung mit dem nationalen Verzehrsmodell NVS II (Lambda- Cyhalothrin) Rückstand Bevölkeru ngsg ru ppe Perzentil (mg/kg) Variabili- Fall %der ARfD tätsfaktor Guave, verarbeitet deutsche Kinder, MAX 2-4 Jahre (3 Personentage) 0,06 1 3 <1% Guave, roh erwachsene deutsche MAX Gesamtbevölkerung, 14-80 Jahre (2 Personentage) 0,06 7 2a 15% Expositionsschätzung mit Version 3 des EFSA PRIMo (Lambda-Cyhalothrin) Bevölkerungsgruppe Perzentil Rückstand (mg/kg) Variabili- Fall %der ARfD tätsfaktor Kinder, Niederlande Geschätzt 0,06 7 erwachsene Geschätzt 0,06 polnische Gesamtbevölkerung 7 2a 2a 26% 21% Expositionsschätzung mit Version 18 des FAO/WHO IESTI Modells (Lambda- Cyhalothrin) Bevölkeru ngsg ru ppe Erwachsene, brasilianische Gesamtbevölkerung (398 Personentage) Rückstand Perzentil (mg/kg) 97,5 0,06 Variabilitätsfaktor Fall %der ARfD 3 (Modell-basiert) 2a 20% 7 (EU Standard- annahme) 2a 30%
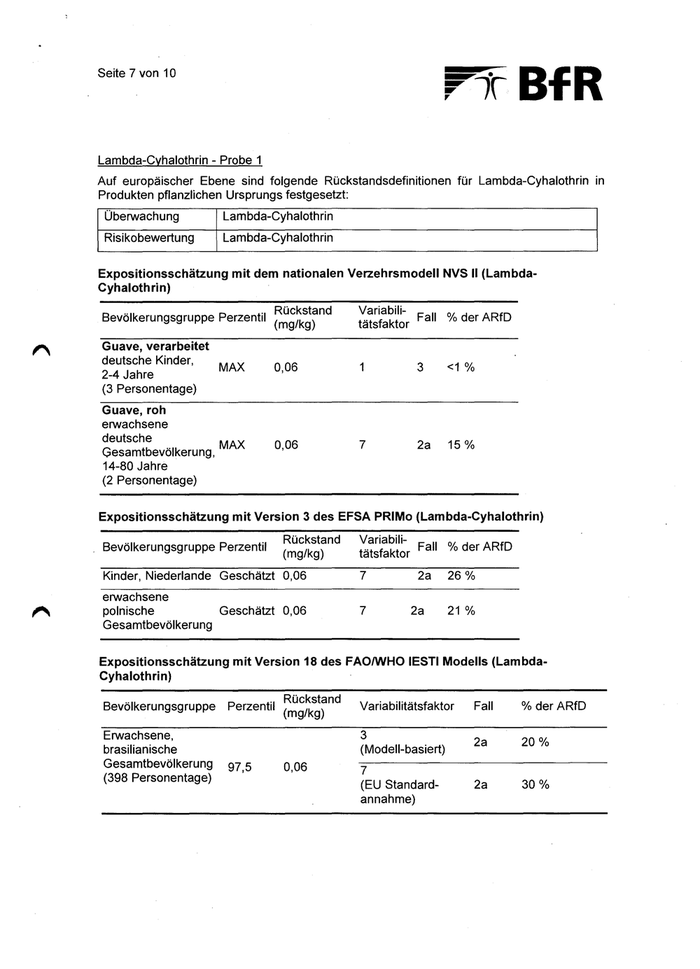
Seite 8 von 10 Basierend auf den maximal nachgewiesenen Lambda-Cyhalothrin-Rückständen in Guave wird die ARfD für keine der berücksichtigten Verbrauchergruppen durch Probe 1 überschritten. Dimethoat und Omethoat - Proben 2 und 3 Auf europäischer Ebene sind folgende Rückstandsdefinitionen für Dimethoat und Omethoat in Produkten pflanzlichen Ursprungs festgesetzt: Überwachung Dimethoat Omethoat Mit Verordnung (EU) Nr. 2017/1135 wurden erstmals gesonderte Rückstandshöchstgehalte für beide Stoffe festgesetzt. Risikobewertung Summe aus Dimethoat + Omethoat x TEF*, berechnet als Dimethoat-Äquivalente * TEF = toxikologischer Äquivalenzfaktor (chronisch = 3, akut= 6) Der in Hinblick auf mögliche Verbraucherrisiken durch den einmaligen Verzehr der am höchsten belasteten Guavenprobe zu bewertende Rückstand beträgt somit 7 0,305 mg/kg Dimethoat-Äquivalente (0,026 mg/kg + 0,043 x 1,08 mg/kg x 6). Expositionsschätzung mit dem nationalen Verzehrsmodell NVS II (Dimethoat + Omethoat) Bevölkerungsgruppe Perzentil Rückstand in Dimethoat- Äquivalenten (mg/kg) Variabili- tätsfaktor Fall %der ARID Guave, verarbeitet deutsche Kinder, 2-4 Jahre (3 Personentage) MAX 0,305 MAX 0,305 3 <1% 2a 37% Guave, roh erwachsene deutsche Gesamtbevölkerung, 14-80 Jahre (2 Personentage) 7 7 Korrekturfaktor aus den Molmassen für Dimethoat (229,3 g/mol) und Omethoat (213,2 g/mol) V
Seite 9 von 10 Expositionsschätzung mit Version 3 des EFSA PRIMo (Dimethoat + Omethoat) Bevölkerungsgruppe Perzentil Rückstand in Dimethoat- Äquivalenten (mg/kg) Kinder, Niederlande Geschätzt 0,305 7 2a 67% erwachsene polnische Gesamtbevölkerung Geschätzt 0,305 7 2a 54% Variabili- tätsfaktor Fall % derARfD Expositionsschätzung mit Version 18 des FAO/WHO IESTI Modells (Dimethoat + Omethoat) Bevölkerungsgruppe Perzentil Rückstand in Dimethoat- Äquivalenten (mg/kg) erwachsene brasilianische Gesamtbevölkerung Variabili- tätsfaktor Fall % derARfD 3 (Modell- basiert) (398 Personentage) 97,5 0,305 2a 60% 2a 90% 7 (EU Standard- annahme) Basierend auf den maximal nachgewiesenen Dimethoat- und Omethoat-Rückständen in Guave wird die ARfD für Dimethoat für keine der berücksichtigten Verbrauchergruppen durch Probe 2 oder Probe 3 überschritten. 3.3 Gesundheitliche Bewertung Sofern die geschätzte Aufnahme oberhalb der ARfD eines Stoffes liegt, ist eine akute gesundheitliche Beeinträchtigung grundsätzlich möglich. ln den übrigen Fällen ist eine gesundheitliche Beeinträchtigung praktisch ausgeschlossen. Unter Berücksichtigung der individuellen ARfDs für die nachgewiesenen Wirkstoffe ergibt die Abschätzung der akuten Exposition auf Basis deutscher, europäischer und brasilianischer Verzehrsdaten für Guave sowohl bei Kindern als auch bei Erwachsenen keine Überschreitung der ARfD. Eine gesundheitliche Beeinträchtigung durch die Einzelstoffe wird praktisch ausgeschlossen. Abschätzung des kumulativen Kurzzeitrisikos Ergänzend wurde jedoch festgestellt, dass in Probe 1 zwei Wirkstoffe mit neurotoxischem Potential (Chlorpyrifos und Lambda-Cyhalothrin) nachgewiesen wurden, für welche eine additive Wirkung zum gegenwärtigen Zeitpunkt nicht ausgeschlossen werden kann. Die kumulative Bewertung basierend auf den berechneten Aufnahmemengen für die Einzelstoffe ergibt einen Hazard Index (HI) von 1,01 für Kinder aus den Niederlanden ([75 % ARfD Chlorpyrifos + 26% lambda-Cyhalothrin]-;- 100) sowie von 1,3 für Erwachsene auf Basis brasilianischer Verzehrsdaten ([1 00 % ARfD Chlorpyrifos + 30 % lambda-Cyhalothrin] -;- 100).

Seite 10 von 10 Bei einer Überschreitung des Hl von 1 ist ein kumulatives gesundheitliches Risiko grundsätzlich möglich. Durch Hemmung der Cholinesterase-vermittelten Inaktivierung des Neurotransmitters Acetylcholin weist Chlorpyrifos eine akute Neurotoxizität auf, die auch als cholinerge oder indirekte parasympathomimetische Wirkung beschrieben wird. Die Symptomatik umfasst zunächst typischerweise vermehrte Speichelbildung und Tränenfluss, Kopfschmerzen, Schwindel- und SchwächegefühL Eine Aufnahme größerer Mengen würde sich in Erbrechen, Koliken (Bauchkrämpfen) und Muskelschwäche bzw. Muskelzittern äußern. Durchfall und Störungen der visuellen Wahrnehmung könnten auftreten. Unbehandelt kann die Symptomatik längere Zeit anhalten, bis das durch Chlorpyrifos inaktivierte Enzym (Cholinesterase) in ausreichenden Mengen nachgebildet wurde. Lambda-Cyhalothrin gehört zur Gruppe der Typ II - Pyrethroide und blockiert als neurotoxische Substanz die spannungsabhängigen Natriumkanäle an den Nervenbahnen. Bei akut toxischer Einwirkung rufen Pyrethroide reversible Reizungen und Rötungen der Haut und Schleimhaut, Kribbeln und Jucken, Augenbrennen, Atemwegsreizungen, Kopfschmerz, Schwindel, Übelkeit und Erbrechen hervor. Als Symptome einer chronischen Einwirkung werden u. a. reversible Sensibilitätsstörungen, Seh- und Hörstörungen, Beeinträchtigung der intellektuellen Leistungsfähigkeit, depressive Verstimmungen und Antriebslosigkeit berichtet. ln dem Entwurf ,Establishment of cumulative assessment groups of pesficides for their effects on the nervaus system' ordnet die EFSA Chlorpyrifos und Lambda-Cyhalothrin verschiedenen Cumulative Assessment Groups (CAGs) zu. Sofern die von EFSA vorgeschlagene Methodologie und Zuordnung bestätigt wird, könnte zukünftig ein ,Refinement' möglich sein. Bis zur Verabschiedung findet dieser Entwurf jedoch keine Anwendung.